Ю.И.ПАХОМОВCборник
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Порядок работы | Задания | Наблюдения и выводы |
|---|---|---|
| Собрать прибор (по схеме),
положить в чашечку немного кристаллической
натриевой (чилийской) селитры, расплавить ее.
Раскалить в пламени спиртовки кусочек
древесного угля и спустить его в расплавленную
селитру
|
Почему вспыхивает уголь? Написать уравнения происходящих реакцийна основе электронного баланса, сделать соответствующие выводы | ... |
| Взять пробы всех трех
растворов в пробирках |
В трех пронумерованных пробирках даны растворы хлорида, сульфата и нитрата натрия. Распознать раствор селитры. Почему к раствору нитрата сначала добавляют концентрированную серную кислоту? Написать молекулярное и ионные уравнения реакции. Проверить вывод реакцией «на следы» с дифениламиновым индикатором | ... |
Сложные вещества (скипидар, древесина,
опилки) тоже могут гореть в азотной кислоте.
Смесь концентрированных азотной и серной кислот
(нитрующая смесь) со многими органическими
веществами образует нитросоединения (реакция
нитрования).
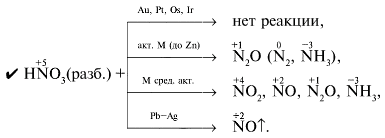
Смесь 1 объема HNO3 (конц.) и 3 объемов HCl (конц.)
называют «царской водкой». В такой смеси
растворяются даже золото Au и платина Pt:
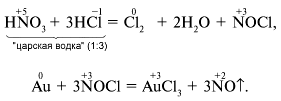
| Порядок работы | Задания | Наблюдения и выводы |
|---|---|---|
| В пробирку с концентрированной азотной кислотой (1 мл) добавить немного медных стружек (Сu). При замедленном эффекте немного подогреть.Работать под тягой! Продукты из санитарной склянки вылить в канализационную систему и смыть струей воды | Чем объясняется выделение бурого газа с резким запахом? Учитывая, что при этом еще образуются вода и нитрат меди(II), написать уравнение реакции. Составить схему электронного баланса и написать уравнение реакции в ионной форме | … |
| Порошок мелкокристаллической серы (S) смешать с 1 мл концентрированной HNO3, подогреть смесь (под тягой). Взять пробу продуктов реакции и испытать ее 2–3 каплями раствора хлорида бария. Продукты из санитарной склянки немедленно вылить в канализационную систему | Чем объясняются наблюдаемые изменения – растворение серы, выделение бурого резко пахнущего газа (и воды)? Написать уравнение данной реакции. Составить схему электронного баланса и иoннoе уравнение реакции. Что доказывают изменения, наблюдаемые при взаимодействии пробы продуктов реакции с раствором хлорида бария? Ответ обосновать | … |
Практическая работа 14.
Определение ортофосфатов
Цели. Научиться распознавать
ортофосфаты, гидроортофосфаты и
дигидроортофосфаты по их растворимости в воде,
гидролизу, качественной реакции на
ортофосфат-анион.
Оборудование и реактивы. Штатив с
пробирками, cтеклянные трубочки с резиновыми
кольцами, санитарная склянка, шпатели (3 шт.);
кристаллические Са3(РO4)2, СаHPO4,
Са(H2РO4)2, дистиллированная вода,
универсальный индикатор, pастворы H3РO4,
NaCH3COO (![]() = 10%),
AgNO3.
= 10%),
AgNO3.
| Порядок работы | Задания | Наблюдения и выводы |
|---|---|---|
| В три пробирки насыпать по 1 см3 ортофосфата, гидроортофосфата и дигидроортофосфата кальция, прилить немного (одинаковое количество) воды, перемешать | Сделать вывод о растворимости первичных, вторичных и третичных ортофосфатов. Можно ли разную растворимость этих фосфатов считать методом их распознавания? | … |
| Используя водные растворы и суспензиив трех пробирках предыдущего опыта, испытать их универсальным индикатором | Определить по шкале pH всех растворов и объяснить, почему pH в этом случае имеет различные значения | … |
| K водному раствору
ортофосфорной кислоты в одной пробирке (1 мл) и раствору суперфосфата в другой (1 мл) добавить 10%-й раствор ацетата натрия и несколько капель нитрата серебра(I) |
Что является
реактивомна ион |
… |
Практическая работа 15.
Определение минеральных удобрений.
Решение экспериментальных задач по теме
«Подгруппа азота»
Цели. Повторить состав и свойства
соединений азота и фосфора, их взаимопревращения
и способы распознавания.
Оборудование и реактивы. Спиртовка,
спички, синее стекло, фильтровальная бумага,
держатель для пробирок, штатив с пробирками (2
шт.), шпатели (3 шт.), ступка, пестик, санитарная
склянка;
в пробирках № 1–3:
I вариант – суперфосфат двойной, NH4NO3,
(NH4)2SO4,
II вариант – NH4Сl, NaNO3, KCl,
III вариант – KNO3, (NH4)2SO4,
суперфосфат двойной;
кристаллические соли (NH4)2SO4,
NH4Сl, аммофос, водные растворы СН3СOONa (![]() = 10%), AgNO3, BaCl2,
= 10%), AgNO3, BaCl2,
СН3СOOH (![]() = 10%),
NaOH, лакмусовая бумажка, CuO, Cu (стружки), HNO3
(разб.), HNO3 (конц.), H2SO4 (конц.),
дифениловый индикатор, (C6H5)2NH в
концентрированной H2SO4,
= 10%),
NaOH, лакмусовая бумажка, CuO, Cu (стружки), HNO3
(разб.), HNO3 (конц.), H2SO4 (конц.),
дифениловый индикатор, (C6H5)2NH в
концентрированной H2SO4,
Ca(OH)2 (сухой), вода дистиллированная, AgNO3
в HNO3, в пробирках № 4–6 сухие
кристаллические вещества: Na2SO4, NH4Cl,
NaNO3, в пробирках № 7 и 8: H3PO4 и H2SO4
Экспериментальная задача. В четырех пронумерованных склянках находятся водные растворы ортофосфата натрия, сульфата аммония, натриевой селитры, хлорида калия. Используя наиболее рациональные методы распознавания (см. табл.), определить, где находится каждое вещество.
Характерные признаки некоторых солей
(методы распознавания)
Таблица
| Название вещества | Внешний вид | Растворимость (в воде) | Взаимодействие раствора данной соли с | Окрашивание пламени | |||
|---|---|---|---|---|---|---|---|
| H2SO4
(конц.) и Cu |
растворами BaСl2 и СН3СООН | раствором NaOH при нагревании | раствором AgNO3 | ||||
| Нитрат аммония NH4NO3 | Белый кристаллический порошок | Хорошая | NO2 |
– | NH3 |
– | Желтое (от примесей) |
| Хлорид аммония NH4Cl | Белый кристаллический порошок | Хорошая | – | – | NH3 |
AgCl |
Желтое (от примесей) |
| Нитрат калия KNO3 | Светло-серые мелкие кристаллы | Хорошая | NO2 |
– | – | – | Фиолетовое |
| Cульфат аммония (NH4)2SO4 | Бесцветные крупные кристаллы | Хорошая | – | BaSO4 |
NH3 |
Ag2SO4 |
– |
| Суперфосфат Са(H2PO4)2• 2H2O | Светло-серый порошок или гранулы | Растворяется медленно | – | Ba3(РO4)2 белый, частично растворим в СН3СООН |
– | Ag3PO4 |
Kирпично- красное |
| Сильвинит KCl•NaCl | Розовые кристаллы | Хорошая | – | – | AgCl |
Желтое с проблесками фиолетового | |
| Хлорид калия KCl | Бесцветные кристаллы | Хорошая | – | – | – | AgCl |
Фиолетовое |
Решение
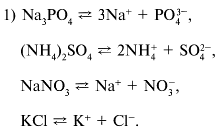
Все ионы в водной среде бесцветные, по
цвету их распознать невозможно.
2) Поскольку ни одно из веществ (склянки № 1–4) не
отличается худшей растворимостью, то и по этому
признаку растворы не отличить, все – прозрачные
растворы.
3) В двух растворах присутствуют одинаковые
катионы, но во всех – различные анионы, поэтому
качественное распознавание следует вести по
анионам. Реактив на ![]() – AgNO3 в присутствии 10%-го
раствора СН3СООNa (или BaCl2 и СН3СООН);
реактив на
– AgNO3 в присутствии 10%-го
раствора СН3СООNa (или BaCl2 и СН3СООН);
реактив на ![]() – раствор BaCl2; реактив на Cl– –
раствор AgNO3 в HNO3; реактив на
– раствор BaCl2; реактив на Cl– –
раствор AgNO3 в HNO3; реактив на ![]() – концентрированная Н2SO4
и Cu (стружки). Можно сразу выявить
– концентрированная Н2SO4
и Cu (стружки). Можно сразу выявить ![]() , затем, используя один реактив
(AgNO3), распознать все три оставшихся
раствора (или наоборот). Другие варианты более
длительны и требуют значительно большего
расхода реактивов.
, затем, используя один реактив
(AgNO3), распознать все три оставшихся
раствора (или наоборот). Другие варианты более
длительны и требуют значительно большего
расхода реактивов.
4) Все четыре пробы растворов испытать раствором
AgNO3 (1–2 капли): раствор из склянки № 4
остался без изменения – это должен быть раствор
NaNO3; в склянке № 2 – белый кристаллический
осадок, нерастворимый в кислотах, – это раствор
KCl; две остальные пробы дают мутные растворы, при
добавлении в которые 10%-го раствора СН3СООNa
проба № 3 дает осадок желтого цвета – это раствор
Na3PO4, а проба № 1 – раствор (NH4)2SO4
(муть исчезает при добавлении кислоты HNO3).
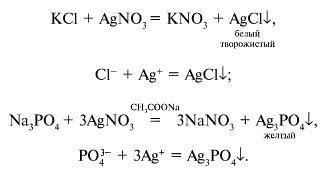
Проверка первичных испытаний.
![]() К пробе раствора из
склянки № 1 добавить по 1–2 капли растворов BaCl2
и СН3СООН, раствор становится молочного
цвета, т. к. выпадает белый кристаллический
осадок:
К пробе раствора из
склянки № 1 добавить по 1–2 капли растворов BaCl2
и СН3СООН, раствор становится молочного
цвета, т. к. выпадает белый кристаллический
осадок:
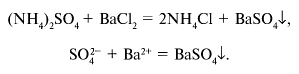
Можно эту же пробу проверить добавлением раствора щелочи с нагреванием. Выделяется газ NH3, определяемый по характерному запаху и посинению влажной красной лакмусовой бумажки. Уравнение реакции:
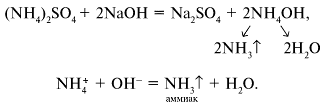
![]() К пробе раствора из
склянки № 4 добавить концентрированную H2SO4
и Cu (стружки), немного подогреть. Выделяется газ
бурого цвета с резким запахом, и раствор
становится зеленовато-лазурного цвета:
К пробе раствора из
склянки № 4 добавить концентрированную H2SO4
и Cu (стружки), немного подогреть. Выделяется газ
бурого цвета с резким запахом, и раствор
становится зеленовато-лазурного цвета:
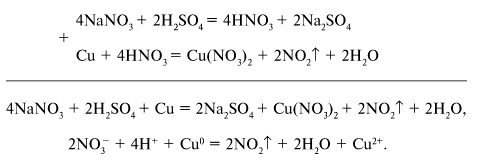
5) Вывод.
В склянках:
№ 1 – раствор (NH4)2SO4,
№ 2 – раствор KCl,
№ 3 – раствор Na3PO4,
№ 4 – раствор NaNO3.
Cхема распознавания
Определяемые растворы |
|||
| № 1 | № 2 | № 3 | № 4 |
| (NH4)2SO4 | KCl | Na3PO4 | NaNO3 |
| Все растворы прозрачные и бесцветные | |||
| +AgNO3 | |||
| Помутнение раствора
(Ag2SO4 в кислотах) |
Белый творожистый
осадок (AgСl |
Мутный раствор, при
добавлении CH3COONa дает желтый осадок Ag3PO4 |
Без изменений |
| +BaCl2 | +H2SO4
(конц.), +Сu (стружки) |
||
| BaSO4 белый, нерастворим в кислотах |
NO2 бурый газ с резким запахом, изменяется цвет раствора (Сu2+) |
||
| Порядок работы | Задания | Наблюдения и выводы |
|---|---|---|
| Используя таблицу, составить план (порядок) распознавания веществ | Согласно варианту записать, растворы каких солей даны в пробирках № 1–3. Определить, где находится каждое из указанных веществ. В выводах записать уравнения проведенных реакций в молекулярной и ионной формах. Отметить признаки каждой качественной реакции | … |
| 1) В пробирку с
небольшим количеством CuO (на кончике шпателя)
добавить раствор HNO3, взболтать. 2) В пробирку с концентрированной HNO3 опустить немного медных стружек (если эффект сразу не наблюдается, немного подогреть смесь) |
Используя выданные
реактивы, получить раствор нитрата меди(II) двумя
способами. Отметить признаки реакций и написать
молекулярные и ионные уравнения реакций. Kакая из реакций является окислительно-восстановительной? |
… |
| В ступке смешать и
растереть смесь Повторить опыт с другими солями аммония |
Опытным путем
доказать, что сульфат, нитрат и хлорид аммония нельзя смешивать с известью. Дать соответствующие объяснения |
… |
| Составить план (порядок) распознавания, наиболее рациональный по времени и расходу реактивов | В пробирках № 4–6
определить кристаллические сульфат натрия, хлорид аммония и нитрат натрия. Написать уравнения реакций. Отметить наблюдаемые признаки реакций |
... |
| Лучше всего испытать
пробы растворов в пробирках № 7 и 8 реактивами BaCl2
и CH3COOH, очень внимательно наблюдая за результатом при взбалтывании реакционной смеси |
Kачественным
распознаванием определить, в какой из пробирок № 7 и 8 находятся растворы серной и ортофосфорной кислот. Написать уравнения реакций |
... |
| Составить план
распознавания веществ Na3PO4 и Сa3(PO4)2 в пробирках № 9 и 10 |
Определить
практически в пробирках № 9 и 10 кристаллические ортофосфаты натрия и кальция |
... |